برقکافت سدیم کلرید
الکترولیز کلرید سدیم یک سیستم حیاتی برای ساخت بسیاری از مواد شیمیایی فله ای است که کاربرد تجاری دارند، مانند کلر، هیدروکسید سدیم و غیره. کلرید سدیم یا در یک قلمرو مذاب یا در محلول های آبی برقکافت می شود. علاوه بر این، برقکافت در حضور نمک های اضافی برای منبع واکنش های ردوکس انجام می شود.
برقکافت سدیم کلرید مذاب
الکترولیز شامل حرکت یون ها به الکترود است. Solid Kingdom دیگر اجازه حرکت یون ها را نمی دهد و برای برقکافت سدیم کلرید نادرست است. هنگامی که در دمای بیش از حد ذوب می شود، سدیم کلرید به یون های سدیم و کلرید جدا می شود، به طوری که برقکافت می تواند مکان اتم های سدیم و بنزین کلر را شکل دهد.
NaCl → Na +(l) + Cl–(l)
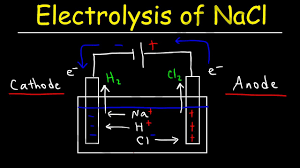
در کاتد: کاهش 2Na+(l) + e-→ Na(l)
در آند: اکسیداسیون 2Cl–(l) → Cl2(g) + 2e–
واکنش خالص به صورت زیر تشکیل شده است: 2Na +(l) + 2Cl-(l) → 2Na(l) + Cl2(g)
فرآیند داون:
کلرید سدیم در دمای کاملاً بالای 801 درجه سانتیگراد ذوب می شود. افزودن انیدرید کلرید کلسیم به نسبت CaCl2: NaCl = سه: 2، فاکتور ذوب را به 580 درجه سانتیگراد کاهش می دهد. الکترولیز با کاتد آهن و آند گرافیت و گاز آهنی انجام می شود که از ادغام کلر و سدیم کالا جلوگیری می کند. کالای کلرید سدیم مذاب فولاد سدیم و گاز کلر است.
برقکافت سدیم کلرید آبی
کلرید سدیم تفکیک شده و به صورت یون های سدیم و کلرید در محلول آبی وجود دارد. برقکافت سدیم کلرید در پاسخ آبی پیچیدگی کمتری دارد. اما خود آب میتواند از طریق واکنشهای کاهش و اکسیداسیون در پتانسیلهای متمایز انجام شود. بنابراین، ماده ای که اکسید می شود یا کاهش می یابد، به تنهایی یون های سدیم و کلرید نیست، اما می تواند مولکول آب را نیز درگیر کند.
دو واکنش رقیب در هر کاتد و آند قابل دوام است. در کاتد: پاسخ کاهشی: در pH = 7
آب ممکن است به گاز هیدروژن یا یون های سدیم به فلز سدیم کاهش یابد.
2H 2 O(l) + 2e– → H 2 (g) + 2OH– E° = -1.0 V
Na+(l) + e– → Na(l) E° = -2.71V
در آند: واکنش اکسیداسیون: در pH = 7. آب ممکن است به اکسیژن یا یون کلرید اکسید شده به مولکول کلر تبدیل شود.
2H 2 O → O 2 (g) + 4H+ + 4e– E° =-1.42 V
2Cl– → Cl 2 + 2e– E =- 1.36V
از این رو، ساخته شده ازبرقکافت سدیم کلرید بی ممکن است یکی از موارد زیر باشد:
ط) فلز سدیم یا بنزین هیدروژن در کاتد و
ب) کلر یا بنزین اکسیژن روی آند،
با یک طرف ساخته شده از هیدروکسید سدیم به دلیل پاسخ سدیم و آب. ساخته شده از برقکافت سدیم کلرید به آگاهی از پاسخ آبی کلرید سدیم بستگی دارد.
الف) محلول آبی بسیار رقیق سدیم کلرید
آب رسانایی بسیار کمی دارد و مقدار کمی کلرید سدیم یونی به هدایت یونی محلول کمک می کند. در غلظتهای کوچک، برقکافت سدیم کلرید آب مهمتر میشود و هیدروژن در کاتد و اکسیژن در آند تولید میشود.
در کاتد: 2H 2 O + 2e– → H 2 (g) + 2OH – E° = -1. صفر V
در آند: 2H 2 O → O 2 (g) + 4H + + 4 e– E° = +1.4 V
پاسخ خالص برقکافت سدیم کلرید آبکی فوقالعاده ضعیف شده به شرح زیر است.
2H 2 O → H 2 (g) + 2OH – + O 2 (g) E° = – 2.4 V
ب) غلظت بالای کلرید سدیم
در کاتد: واکنش تخفیف: در pH = 7
2H 2 O(l) + 2e– → H 2 (g) + 2OH – E° = -1. صفر V
Na+(l) + e– → Na(l) E° = -2.71V
کاهش (بیش از حد) توانایی آب بسیار زیادتر از کاهش یون های سدیم است، آب برای آزاد کردن هیدروژن در کاتد تجزیه می شود.
در آند: واکنش اکسیداسیون: در pH = 7
2H 2 O → O 2 (g) + 4H+ + 4 e– E° =-1.4 V
2Cl – → Cl 2 + 2 e– E =- 1.36V
قابلیت تنزیل ترمودینامیکی آب و کلرید به ترتیب +صفر 82/0 و 36/0 ولت است. اکسیداسیون آب بسیار عالی امکان پذیرتر است و بنابراین، تکامل گاز اکسیژن باید روی آند ظاهر شود. به هر حال، تولید اکسیژن از آب دارای اضافه ولتاژ 0.6 ولت است که ولتاژ اکسیداسیون آب را 1.4 ولت می کند. اکسیداسیون کلرید فوق العاده تر از ولتاژ اینترنت اکسیداسیون آب است. بنابراین، کلرید روی آند به کلر اکسید می شود. مکان گرفتن پاسخ اینترنتی به صورت زیر است.
در کاتد – 2H 2 O (l) + 2e – → H 2 (g) + 2OH –
در آند – 2Cl – → Cl 2 + 2e –
پاسخ استاندارد به شرح زیر است؛
2H 2 O(l) + 2Cl – → H 2 (g) + Cl 2 + 2OH –
یا
2H2O g) + (l) + 2NaCl → H2 ( Cl 2 + 2NaOH
در غلظت بیش از حد نمک، هیدروژن و کلر از برقکافت سدیم کلرید به عنوان یک محصول از طریق برقکافت ساخته می شوند.
در سیستم کاستنر-کلنر، آب نمک (کلرید سدیم آبی) در یک موبایل دارای اطاقک برقکافت می شود. آند گرافیت در داخل محفظه های جانبی و کاتد آهن در محفظه حیاتی قرار دارد. جیوه در پایین است و دو غرفه را از هم جدا می کند و به عنوان مجرای برای پوشیدن سدیم شکل در اطاقک های توقف به محفظه مربوطه عمل می کند.
آب نمک اضافه شده به محفظه توقف، به سدیم و کلر برقکافت می شود. در حالی که کلر از بالای موبایل خارج می شود، سدیم آمالگام سدیم را با جیوه در کمترین مقدار تشکیل می دهد. سدیم انتقال یافته به محفظه بحرانی با آب واکنش می دهد و هیدروکسید سدیم و هیدروژن را شکل می دهد.
مواد ساخته شده از برقکافت کلرید سدیم آبی غلیظ عبارتند از: هیدروکسید سدیم، بنزین هیدروژن و گاز کلر.
جیوه استفاده شده در تکنیک کستر-کلنر محصولات را آلوده می کند و به دلیل تصعید یک شانس محیطی است. جیوه که سرطان زا است، برای برقکافت کلرید سدیم آبکی عقب نشینی می کند.
در حال حاضر تمام صنایع کلر قلیایی که کلر و هیدروکسید سدیم تولید می کنند از یک غشای نیمه تراوا “Nafion” برای جداسازی قسمت های آند و کاتد استفاده می کنند.
Nafion یک کوپلیمر یونی سولفونه تترا فلوئورو-اتیلن است. غشاء به یون سدیم اجازه می دهد تا در سراسر غشاء به داخل سلول کاتد حرکت کند. تقویت اضافی با غشاهای نیمه تراوا مختلف از هرگونه اختلاط برگشتی یون های کلرید و هیدروکسید ورودی در سراسر Nafion جلوگیری می کند.
ج) برقکافت کلرید سدیم آبی در غلظت متوسط
در کاتد: کاهش آب به هیدروژن قابل قبول تر از هیدروژن سدیم است. در تمام پاسخ های آبی، کاهش آب به هیدروژن در مقایسه با کاهش یون سدیم، در کاتد قرار می گیرد. در آند: توانایی اکسیداسیون یون های آب و کلرید تقریباً یکسان است (به ترتیب 1.4- و 1.36 ولت).
در آگاهی بهتر از کلرید سدیم، اکسیداسیون کلرید از نظر سینتیکی مطلوب است، در همان زمان که در غلظت های پایین، اکسیداسیون آب به هیدروژن از نظر جنبشی مطلوب است. در وسط جاده، ذرات آب و کلرید اکسید می شوند. بنابراین، گازهای اکسیژن و کلر به طور همزمان در آند تکامل می یابند.
در کاتد: پاسخ تخفیف: در pH = 7، 2H 2 O(l) + 2e – → H 2 (g) + 2OH –
در آند: پاسخ اکسیداسیون: در pH = 7، 2H 2 O → O 2 (g) + 4H + + 4e –
2Cl – → Cl 2 + 2e –
پاسخ کاهش x سه 6H 2 O(l) + 6e – → 3H 2 (g) + 6OH –
بنابراین، پاسخ اینترنتی این است؛
4H 2 O(l) + 2Cl – → 3H2(g) + 2OH – + Cl 2 + O 2
یا
4H 2 O(l) + 2NaCl → 3H 2 (g) + 2NaOH + Cl 2 + O 2
برقکافت کلرید سدیم در یک محلول آبی با تکیه بر آگاهی نسبی از کلرید سدیم و آب، محصولات فوق العاده ای به دست می دهد. برقکافت از نظر ترمودینامیکی در غلظتهای بسیار کم و بیش از حد کلرید سدیم کنترل میشود و از نظر سینتیکی در غلظتهای میانجی مدیریت میشود.
آیا می خواهید یک IITian باشید؟ خوب، اینجا خبر خوب است. Infinity Learn دارای سابقه تولید 20 درصد IIT در هر سال است. به دوره اختصاصی JEE 2024 ما بپیوندید تا رویای IIT خود را محقق کنید.
سوالات متداول
محصولات حاصل از برقکافت NaCl چیست؟
محصول برقکافت کلرید سدیم آبی غلیظ هیدروکسید سدیم، گاز هیدروژن و گاز کلر است.
برقکافت آب شور چیست؟
برقکافت آب نمک در شیمی، برقکافت روشی است برای جداسازی عناصر و ترکیبات پیوندی با عبور جریان الکتریکی از آنها. یک ترکیب یونی، در این مورد نمک، با یک حلال مناسب مانند آب حل می شود تا یون های آن در مایع موجود باشد.